ジャクソン研究所の研究者が超希少な遺伝性疾患の症状を緩和することに成功
Media Release
カテゴリー:希少疾患
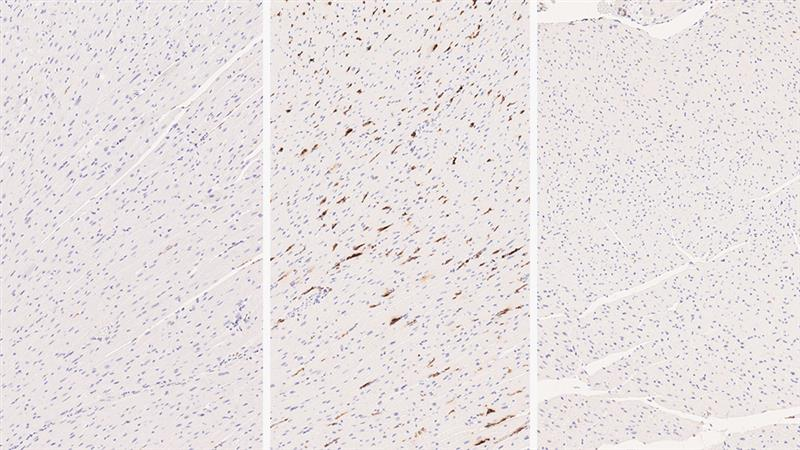
健康なマウスの心臓組織(左)とMSDマウスの心臓組織(中央)。健康なマウスからの骨髄移植により、病気の心臓組織が回復し(右)、MSDマウスの症状が緩和された。
遺伝子治療と骨髄移植を組み合わせることで、多発性スルファターゼ欠損症の包括的な治療ソリューションを提供できる可能性がある
【メイン州バーハーバー 2025年1月28日】ジャクソン研究所(JAX)の研究者らは、2つの新しい論文で、遺伝子治療と骨髄移植という2つのアプローチを用いることで、治療法のない極めて稀な遺伝病である多発性スルファターゼ欠損症(MSD)の症状緩和に成功したと報告しています。マウスを使用して行われたこれらの研究は、MSDの子どもとその家族に新たな希望を与えるだけでなく、関連する遺伝子変異を伴う、より一般的な病気を研究者が理解するのにも役立ちます。
「この研究は、MSDの治療に複数の新しいアプローチを提供するものであり、それらは互いに補完し合う可能性があります。このような複雑な疾患の場合、1つのアプローチだけに頼ることはできません」と、 Dr. Maximiliano Presa (マキシミリアーノ・プレサ)は語りました。彼はMSDのような研究が不十分で資金も不足している希少疾患に関する前臨床研究を加速させるJAXの 希少疾患トランスレーショナル研究センター (Rare Disease Translational Center)のSenior Study Directorです。
この遺伝子治療を利用したアプローチは現在、NIH財団(FNIH)が運営する官民パートナーシップの一環として、ヒトを対象とした臨床試験へと移行しつつあります。
希少疾患に焦点を当てる
MSDを持って生まれた赤ちゃんの平均寿命は13年で、進行を遅らせたり止めたりする治療法は今のところありません。MSDは、細胞が複雑な糖や脂肪を分解するために必要なタンパク質をコードするSUMF1遺伝子の変異によって引き起こされます。糖や脂肪は細胞内に蓄積し、最終的には細胞が正常に機能しなくなります。患者のSUMF1遺伝子の変異の種類に応じて、この蓄積は脳、肝臓、皮膚、骨格に影響を及ぼし、発作、発達遅延、運動障害などの症状が現れることがあります。
Dr. Cat Lutz (キャット・ラッツ)の研究室で働いていたDr.プレサは、MSD治療への新しいアプローチの先導役になりたいと考えていました。この取り組みは、ユナイテッドMSD財団(United MSD Foundation)とJAXの精密遺伝学センター( Center for Precision Genetics )の両方から資金提供を受けました。JAXの精密遺伝学センターは、CRISPR/Cas9などの高度な遺伝子ツールや技術を活用し、希少疾患の研究に用いるマウスモデルを作製しています。また、JAXの精密遺伝学センターは国立衛生研究所(NIH)の支援を受けています。
「希少疾患トランスレーショナル研究センターで私たちが関わっている多くの家族は、深刻な診断に直面しています。その多くは確実に死に至るもので、治療の選択肢はありません。新しい治療法は、これらの家族の希望です。私たちの遺伝子組み換えマウスは、そうした最先端の治療法をテストする上で完璧なモデルです」と希少疾患トランスレーショナル研究センターのVice PresidentであるDr.ラッツは述べました。
新しい骨髄の検査
Communications Medicine 10月25日号 に掲載された研究で、Dr.プレサ、Dr.ラッツと共同研究者は、MSDの治療に骨髄移植を使用する方法を発表しました。このアプローチでは、患者の骨髄を、正常に機能するSUMF1遺伝子を含むドナーの骨髄細胞と入れ替えます。成功すれば、正常に機能するSUMF1遺伝子を持つドナー細胞は体内を移動し、正常な活性を有するスルファターゼを生成します。その後、このスルファターゼは患者の他の細胞に取り込まれ、毒性代謝物の除去に役立ちます。これはcross-correctionと呼ばれる現象です。
研究チームは、JAXで開発された、MSD患者の一部に見られるのと同じSUMF1変異を持つマウスモデルを使用して、機能不全だったタンパク質が骨髄移植によって回復し、さらに肝臓や心臓などの末梢臓器における毒性を伴う糖と脂肪の蓄積が軽減され、炎症と細胞損傷の程度が小さくなることを発見しました。しかし、この治療はMSDの症状の多くの発生源である脳にはほとんど効果がありません。この一因は、細胞に血液脳関門を通過させることが困難なためです。
「ドナー細胞の一部が脳に移動した可能性はありますが、大きな効果があったと確信できるほどの変化は、脳内の分子に見られませんでした。克服する方法を引き続き模索する必要があります」とDr.プレサは説明しました。
欠陥遺伝子の入れ換え
Communications Medicine 1月27日号 に発表された2つ目の研究では、Dr.プレサとDr.ラッツの研究グループは、脳を標的としたMSDのより効果的な遺伝子治療法を開発しました。遺伝子治療では、遺伝子をコードするDNAをデリバリーシステム(通常は小さなウイルス外殻)の中に入れ、健康な遺伝子を送達します。デリバリーシステムは体内を移動し、その中身を体の細胞に注入することができます。
これまでの試みでは複数回の治療が必要で、効果も軽微なものでした。脳脊髄液を通して遺伝子治療を行う新しい方法では、生後1週間で治療を受けたマウスに、寿命の延長(30日から18か月以上)や神経症状の軽減など、大きな改善が見られました。
肝臓などの臓器への影響は細胞の代謝回転により、それほど長く続かない可能性がありますが、脳細胞は頻繁に入れ替わる細胞ではないため、遺伝子治療が脳細胞に与える影響は長続きするとDr.プレサは指摘しました。さらに、この治療法では、わずかな割合の脳細胞(約10%)で正常に機能するSUMF1が低レベルに認められるだけでも症状を改善できることが示されました。
「これは重要な結果です。MSDに効果をもたらすために、子供の脳に信じられないほど大量の遺伝子治療を施す必要はないのです」と彼は語りました。
臨床現場へ
JAXの研究チームがマウスでテストしたどちらのアプローチも、ただちに単独でMSDの治療法にはならず、また病気を生涯にわたり完全に治療できるというわけではないでしょう。遺伝子治療は脳と神経系に効果的ですが、骨髄移植は、他の臓器をより効果的に標的にして治療できる、より高度な細胞ベースの治療法の開発に向けた基礎的なステップとなります。最終的には、研究者は2つの治療法について並行して試験を行うことを決定することになるかもしれません。
「将来的には、遺伝子治療と細胞治療を組み合わせることが、持続的な治療を確実にする方法となるかもしれません。まだ研究が始まったばかりですが、最終的にはこれらの治療法を補完する可能性のある他の種類の遺伝子治療や遺伝子編集もあります」とDr.プレサは語りました。
JAXの研究チームが開発したMSD治療のための遺伝子治療法は、2023年にFNIHの臨床試験ポートフォリオに含まれる 8つの希少疾患治療薬の1つに選ばれました 。これにより、ヒトを対象としたこの治療薬の最初の臨床試験の実施が承認される道筋が整い、患者に新しい治療法をより早く提供できます。
MSDの子供を持つ親たち、たとえば娘のウィローがMSDを持って生まれたアンバー・オルセンや息子のディランがMSDを持って生まれたアラン・フィングラスは、MSD研究を支持し、世界中の科学者と協力して前臨床および臨床試験を進めてきました。オルセン氏とフィングラス氏は、United MSD Foundationへの活動参加を通じて、JAXにおける最近のMSD研究に大きな活力を与えてきました。
ジャクソン研究所について
ジャクソン研究所は独立した非営利の生物医学研究機関であり、米国国立癌研究所指定のがんセンターを有し、米国、日本、中国の各地に約3,000名の従業員を擁しています。その使命は、疾患に対する精密なゲノムソリューションを探索し、世界中の生物医学コミュニティに活力を与えることです。その根底にあるのは「人々の健康を改善したい」という私たち皆の探求心です。詳細については、 www.jax.org をご覧ください。
JAXメディア担当:Cara McDonough cara.mcdonough@jax.org
英語原文: JAX researchers alleviate symptoms of ultra-rare genetic disease at the Jackson Laboratory