ミトコンドリアが供給するエネルギーが血液の病気を引き起こす
Media Release
ジャクソン研究所(JAX)の科学者たちは、ミトコンドリアが供給するエネルギーが血液の病気を引き起こす原因であることを明らかにし、さらにそのエネルギー供給を止める方法も発見しました。
【メイン州バーハーバー 2025年4月16日】加齢に伴い、体内の新しい血液細胞の源として不可欠な血液幹細胞に遺伝子変異が蓄積することがあり、それが細胞の増殖優位性を高め、深刻な疾患の発症リスクを高めることが知られています。JAXの研究チームは今回、こうした血液幹細胞の制御不能な増殖を促進するメカニズムを解明し、さらにそのプロセスを抑制する方法を発見しました。
JAXのProfessorでありダッテルズ・ファミリー寄付講座の主任研究者を務めるDr. Jennifer Trowbridge(ジェニファー・トローブリッジ)が率いるこの研究は、2025年4月16日号の Nature Communications で報告されました。この研究では、Dnmt3a遺伝子に加齢とともに起こる一般的な変異が、血液幹細胞のミトコンドリアのエネルギー産生機能を高めることが明らかになりました。この変異により、細胞は通常よりも容易に自身のコピーを作れるようになり、心臓病や血液がんなどの病気のリスクを劇的に増大させるクローン性造血が起こりやすくなることが示されました。
クローン性造血は、年齢とともに症状を伴わずに発生する現象で、80歳以上の人の半数以上に認められると推定されています。この状態では、変異した血液幹細胞は炎症を引き起こす物質(炎症性分子)を産生することがあります。その結果、正常な血液の産生が妨げられたり、免疫機能が低下したりする可能性があるのです。
「この研究によって、加齢により血液幹細胞がどのように変化するのか、そしてその変化が、がん、糖尿病、心臓病などの病気のリスクをどのように高めるのかについて、新たな理解が得られました。さらにこの発見は、血液だけでなく、血液が流れるすべての組織や臓器において、加齢に伴う病気の進行を食い止めたり予防したりする新たな可能性を示しています」と、Dr.トローブリッジは述べています。
一般的な遺伝子変異
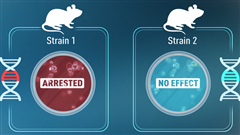
Dr.トローブリッジの研究チームは、これまでの研究から、血液幹細胞のDnmt3a遺伝子の変異が加齢に伴って高頻度に見られること、また血液がん患者でも頻繁に見られることをすでに把握していました。そこで研究チームは、この変異を持つ細胞が、なぜ正常な細胞よりも競合において優位に立てるのかを明らかにするために、Dnmt3a変異を持つマウスモデルを開発しました。
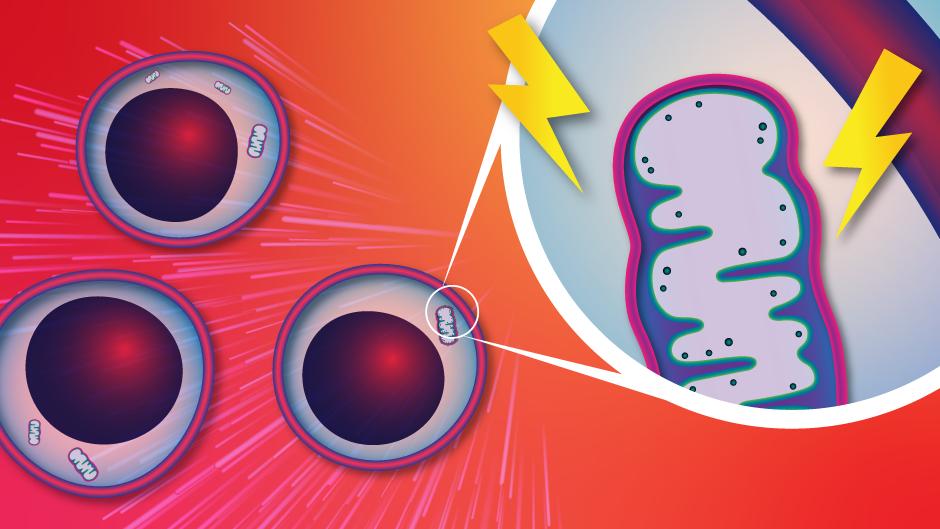
今回の新しい研究で、Dr.トローブリッジのチームは、中年期のマウスにおいて、Dnmt3a変異を持つ血液幹細胞が、正常な幹細胞の約2倍のエネルギーを生み出す能力を持っていることを発見しました。さらに、これらの変異幹細胞ではミトコンドリアの機能亢進が認められ、それにより細胞の増殖において強い優位性を発揮していることが明らかになりました。
「これは本当に予想外の発見でした。これまで、Dnmt3a遺伝子が代謝やミトコンドリアに影響を与えるとは考えられていませんでした」と、Dr.トローブリッジは語っています。
ミトコンドリアを標的にする
研究チームは、Dnmt3a変異を持つ幹細胞が、過剰に活性化したミトコンドリアに強く依存して増殖していることに気づきました。このことから、ミトコンドリアが変異細胞の「アキレス腱」になり得るという視点が浮かび上がりました。そこでチームは、Dnmt3a変異を持つマウスと単離した幹細胞を用いて、ミトコンドリアの正常な機能を妨げる分子「MitoQ」と「d-TPP」の効果を検証しました。これらの分子は、ミトコンドリアの正常な働きを阻害し、エネルギー産生を抑える作用があります。さらに、Dr.トローブリッジと共著者らは、2025年4月16日付の Nature に掲載された別の論文で、2型糖尿病の治療薬として広く使われている「メトホルミン」にも、Dnmt3a変異を持つ幹細胞の競合における優位性を低下させる効果があることを報告しています。
Dnmt3a遺伝子に変異があり、クローン性造血を起こしているマウスに対して、ミトコンドリアを標的とした薬剤を投与したところ、非常に顕著な効果が見られました。投与を始めてわずか数日で、変異を持つ細胞の約半数が死滅し、生き残った細胞でもエネルギー産生が正常なレベルにまで低下しました。一方で、同じ代謝経路にそれほど依存していない正常な幹細胞には影響が見られませんでした。
「突然変異を起こした細胞だけが弱まり、正常な幹細胞には影響がないという、この選択的な脆弱性を目の当たりにして、本当に興奮しました」と、Dr.トローブリッジは語っています。
ヒトの病気に応用できる可能性
このミトコンドリアを標的とした治療薬は、クローン性造血を起こしたマウスだけでなく、DNMT3A遺伝子に変異を持つように操作されたヒトの血液幹細胞でも効果を発揮しました。この結果は、血液がんやその他の加齢に関連する疾患の予防・治療において、この戦略がクローン性造血を呈するヒトにも応用できる可能性を示しています。
しかし、これらの薬剤がクローン性造血で見られる他の種類の遺伝子変異にも有効かどうか、また薬剤が細胞に及ぼす影響を理解するためには、さらなる研究が必要です。
ジャクソン研究所について
ジャクソン研究所(JAX)は、米国国立癌研究所指定のがんセンターを有する独立した非営利の生物医学研究機関です。研究、教育、リソースの独自の組み合わせを活用して、その大胆な使命を達成しています。その使命とは、疾患に対する精密なゲノムソリューションを探索し、世界中の生物医学コミュニティに活力を与えることです。その根底にあるのは「人々の健康を改善したい」という私たち皆の探求心です。1929年にメイン州バーハーバーに設立されたJAXは、メイン州、コネチカット州、カリフォルニア州、フロリダ州、日本の各施設で約3,000名の従業員を有するグローバルな研究機関です。詳細については、 www.jax.org をご覧ください。
JAXメディア担当:Cara McDonough cara.mcdonough@jax.org
英語原文: Supercharged mitochondria spark aging-related blood disorders