糖尿病リスク遺伝子が細胞のストレスに対する回復力を低下させる仕組み
Featured Article

ジャクソン研究所の研究者らは、糖尿病になりやすい遺伝的要因の一部によって、膵臓細胞の分子ストレスに対する反応が変わる可能性があることを発見した。
【コネチカット州ファーミントン 2024年10月8日】膵臓の細胞は、人間と同様に、一定以上のストレスを受けると壊れ始めます。炎症や高血糖などの特定のストレス要因は、膵臓の細胞に負担をかけ、2型糖尿病の発症に寄与します。
ジャクソン研究所(JAX)の研究者らは、糖尿病リスクを高めることが知られている DNA配列の変化が、2種類の分子ストレスに膵臓細胞が対処する能力に関係していることを発見しました。これらのDNA変異を持つ人は、膵臓のインスリン産生細胞がストレスや炎症にさらされると機能不全に陥ったり、死滅したりする可能性が高くなります。
「最終的には、2型糖尿病に最もかかりやすい人々の遺伝子と経路の乱れを標的にして、この病気の予防と治療の新しい方法を開発したいと考えています。この発見は、そうした遺伝子と経路のいくつかについて新たな知見を与えてくれます」と語るのは、JAXのAssociate Professorの
Dr. Michael L. Stitzel
(マイケル・L・スティッツェル)です。彼は、JAXのProfessorである
Dr. Duygu Ucar
(ドゥユグ・ウカル)とともに10月8日付のCell Metabolismオンライン先行公開版で発表された新しい研究の共同上席著者です。
この研究では、細胞ストレスと糖尿病リスクを結びつける数十の遺伝子が挙げられており、その中には2型糖尿病の合併症に対する薬剤ターゲットとして既に研究が進んでいる遺伝子も含まれています。
ストレスを受けた細胞
生きた細胞は、損傷、炎症、栄養の変化などの問題に直面すると、ストレスに対処して回復しようと保護反応を活性化します。しかし、時間が経つと、持続的なストレスに細胞が耐えられなくなり、動きが鈍くなったり、死滅したりすることがあります。
膵臓の膵島ベータ細胞では、2種類の細胞ストレスが2型糖尿病の発症に関係していることがこれまでに指摘されています。
- 小胞体(ER)ストレスは、血糖値の調節を助けるインスリンなどのタンパク質を生成する高い需要に細胞が耐えられなくなったときに発生します。
- サイトカインストレスは、肥満や代謝性疾患などで起こるように、免疫系が過剰な炎症シグナルを送ったときに発生します。
どちらの場合も、ストレスにより、最終的に膵島ベータ細胞がインスリンの生成を停止したり、細胞自体が死滅したりする可能性があります。
Dr.スティッツェルと研究チームは、ERストレスとサイトカインストレスの両方に対処するために膵島細胞が使用する遺伝子とタンパク質を知りたいと考えました。
「過去に実施された複数の研究において、ストレスのない健康な膵島細胞においてインスリン産生を調節する際に重要とされる分子経路が検討されています。しかし、私たちは膵島細胞が常にストレスフリーであるとは限らないという仮説に基づいて研究を行いました。では、細胞がストレスを受けているときに重要な経路はどれなのでしょうか、そして私たち一人ひとりの糖尿病に関連するDNA配列の変化は、そうした細胞にどのような影響を与えるのでしょうか」とDr.スティッツェルは問いかけました。
ストレス反応遺伝子
Dr.スティッツェルの研究グループは、健康なヒトの膵島細胞を、ERストレスまたはサイトカインストレスを引き起こすことが知られている化合物に曝露しました。そして、RNA分子レベルでの細胞内の変化と、細胞内部のさまざまなDNA配列の密度を調べました。この密度は、ある時点で膵島細胞がどの遺伝子と調節エレメントを使用しているかを示す指標となります。研究チームは結果を分析するために、JAXのProfessorで計算生物学者のDr.ウカルと共同作業を行いました。研究グループのメンバーは、健康な膵島細胞で発現する遺伝子のほぼ3分の1にあたる5,000以上の遺伝子が、ERストレスまたはサイトカインストレスに反応して発現を変化させることを発見しました。その多くは、膵島細胞のインスリン産生に不可欠なタンパク質の生成に関与していました。また、遺伝子のほとんどが、どちらか一方のストレス反応にのみ関与していたため、2つの異なるストレス経路が糖尿病に関与しているという考えが浮かび上がりました。
さらに、膵島細胞で一般的に使用されるDNAの調節領域の約8分の1がストレスによって変化していました。重要なことは、これらの調節領域のうち86について、2型糖尿病のリスクが最も高い人々で遺伝子変異が認められることが以前に判明していたことです。
「このことから、これらの遺伝子変異を持つ人は、他の人よりもストレスに対する膵島細胞の耐性が低い可能性があることがわかります。2型糖尿病の引き金を引くのは糖尿病や肥満などの環境ですが、弾を込めるのは遺伝子なのです」とDr.スティッツェルは言います。
Dr.スティッツェルは、この調節領域と遺伝子の新しいリストが、ストレスに対する膵島細胞の回復力を高めることにより、糖尿病を予防または治療する新薬の開発につながることを期待しています。
薬物治療のターゲット
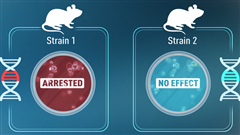
研究者らは、ERストレスとサイトカインストレスの両方によって変化する1つの遺伝子に着目しました。MAP3K5と呼ばれるこの遺伝子は、インスリンをコードする遺伝子に糖尿病を引き起こす変異を持つマウスの膵島ベータ細胞の死を変化させることが示されました。
新しい論文で、Dr.スティッツェルと彼の研究チームは、MAP3K5のレベルが高いと、ERストレスに反応して死滅する膵島ベータ細胞が増えることを示しました。一方、MAP3K5を排除または阻害すると、膵島細胞はERストレスに対してより高い回復力を持ち、死滅する可能性が低くなりました。
MAP3K5を標的とする薬剤であるセロンセルチブの初期研究では、セロンセルチブは糖尿病の重篤な合併症のリスクを軽減する可能性があることが示されています。そして新しい研究結果は、この薬剤の別の可能性を示唆しています。それは、糖尿病リスクが最も高い人の発症を予防し、ストレスを受けても膵島細胞が機能し、生き続けるのを助けるという作用です。
「この治療薬がすでに臨床試験段階にあることは非常に喜ばしいことですが、この薬が一次予防に活用できるかどうかを理解するにはさらに多くの研究が必要です」とDr.スティッツェルは語りました。
ジャクソン研究所について
ジャクソン研究所は独立した非営利の生物医学研究機関であり、米国国立癌研究所指定のがんセンターを有し、米国、日本、中国の各地に約3,000名の従業員を擁しています。その使命は、疾患に対する精密なゲノムソリューションを探索し、世界中の生物医学コミュニティに活力を与えることです。その根底にあるのは「人々の健康を改善したい」という私たち皆の探求心です。詳細については、 www.jax.org をご覧ください。
JAXメディア担当:Cara McDonough cara.mcdonough@jax.org
英語原文: How diabetes risk genes make cells less resilient to stress